[더리포트] 국내연구진이 DNA 염기 하나만을 바꾸는 유전체 교정 도구 ‘Cpf1 기반 염기교정 유전자 가위(Cpf1-linked base editors, 이하 염기교정 유전자 가위)’의 정확성을 최초로 입증하는데 성공했다.
이 연구를 통해 염기교정 유전자 가위의 성능과 정확성이 확인됨에 따라 이를 이용한 유전자 교정기법이 유전자치료 등에 널리 사용될 것으로 기대된다.
이 연구는 한국생명공학연구원(원장 김장성, 이하 생명연) 유전체교정연구센터 김대식 박사팀(교신저자 겸 제1저자: 김대식 박사)과 기초과학연구원(IBS, 원장 노도영) 유전체 교정 연구단 김진수 수석연구위원 연구팀 (교신저자 : 김진수, 공동 제1저자 : 임가영)이 공동으로 수행했다.
아울러 기초과학연구원(IBS) 및 국가과학기술연구회가 추진하는 창의형 융합연구사업(CAP)의 지원을 받았다.
14일 기초과학연구원(IBS, 원장 노도영)에 따르면 생명체에 대한 모든 정보를 담고 있는 DNA는 네 개의 염기로 구성되어 있다. 아데닌(A), 티민(T), 시토신(C), 구아닌(G) 염기는 서로 쌍을 이뤄 순서를 만들고 3개의 염기를 조합해 코돈(Codon)으로 유전 정보를 저장한다. DNA 염기서열이 중요한 이유는 단일 염기 하나만 잘못 되어도 심각한 병을 초래하기 때문이다. 낭성 섬유증, 겸상 적혈구 빈혈증 등은 특정 염기 하나가 잘못되어 발생하는 대표적인 유전질환이다.
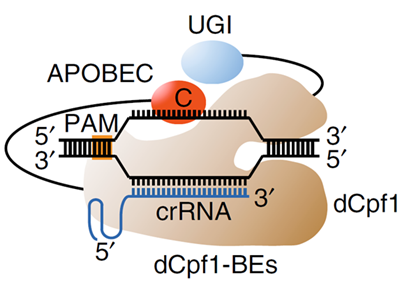
이러한 질환을 치료하기 위해 크리스퍼 유전자가위(CRISPR/Cas9 혹은 CRISPR/Cpf1)를 사용하려는 연구가 많이 진행되었으나, 이는 DNA 염기서열을 잘라 유전자가 작동을 하지 못하게 하는 일은 가능하지만 특정 염기를 바꾸어 주는 것에는 어려움이 있었다.
이를 보완하기 위해 염기교정 유전자 가위(Cpf1 시토신 염기교정 유전자가위)가 개발되었으나, 염기교정 유전자가위가 표적 위치에 정확히 작동하는지, 비표적 위치에 오작동하지 않는지는 전혀 알려지지 않았었다.
연구진은 자체 개발한 절단 유전체 분석 기법(Digenome-seq)1) 으로 세계에서 처음으로 유전체 전체 수준에서 염기교정 유전자가위가 비표적 위치에서 오작동이 일어나는 위치를 확인, 그 정확성을 규명했다.
연구책임자인 김대식 박사는 “이번 연구성과는 염기교정 유전자가위의 정확성을 측정한 결과, 염기교정 유전자가위의 DNA에서 오작동이 일어나는 위치가 유전자가위와 다른 것을 확인 한 성과”라고 밝혔다.
이어 “이번 연구에서 Cpf1 시토신 염기교정 유전자가위를 구성하는 탈아미노효소에 변이를 줌으로써 정확성이 더 높은 크리스퍼 염기교정 유전자가위를 제작하였고, Cpf1 시토신 염기교정 유전자가위의 성능이 확인됨에 따라 향후 이 기술은 유전자 및 줄기세포 치료제 개발, 고부가가치 농축산물 품종 개량 등 널리 활용될 것으로 기대된다.”고 덧붙였다.
이 연구는 생물학 분야의 세계적 저널인 네이쳐 커뮤니케이션지(Nature Communications, IF 11.878) 8월 13일자 온라인 판에 게재되었다. (논문명 : Genome-wide specificity of dCpf1 cytidine base editors)
