기초과학연구원(IBS) 시냅스 뇌질환 연구단
뇌 발달 및 기능 조절에서 TANC2 단백질 중요성 규명

[더리포트=이진수 기자] 국내연구진이 자폐 및 뇌 발달장애를 유발하는 새로운 매커니즘을 규명했다.
기초과학연구원(IBS)은 15일 연구원 소속 시냅스 뇌질환 연구단 김은준 단장 연구팀이 최근 자폐 및 뇌 발달장애의 원인으로 부상한 TANC2 유전자 변이의 발병 메커니즘을 밝혔다고 전했다.
이로써 TANC2 유전자 돌연변이에서 기인한 자폐 및 뇌 발달장애 치료제 개발에 크게 기여할 것으로 기대된다.
기초과학연구원에 따르면 자폐증(Autism spectrum disorders)은 뇌 발달장애의 한 종류로서, 세계 인구의 약 2%가 앓고 있다. 뇌의 발달은 세포 내 다양한 신호전달(signaling) 체계에 의해 조절된다. 그중 ‘mTOR 신호전달2)은 신경세포를 포함한 대부분 세포의 발달과 기능을 제어한다. 여기에는 대사 장애, 뇌 발달장애 등 다양한 질환이 관련되어 있다고 알려져 있다. 그러나 신경계에서의 mTOR 조절 기전은 이제까지 알려진 바가 거의 없었다.
시냅스 뇌질환 연구단은 이전 연구에서 ‘TANC2 단백질 TANC2 단백질3)’이 정상적인 뇌 발달에 필수적임을 규명했다. 이후 다양한 임상연구를 통해 TANC2와 자폐 및 뇌 발달장애의 연관 가능성이 제기되었다. 다만 정확한 발병기전을 밝히지는 못했다. 이번 연구에서는 TANC2 단백질이 mTOR 단백질의 직접 억제자(negative regulator)로서 뇌 발달 및 기능을 조절함을 규명했다.
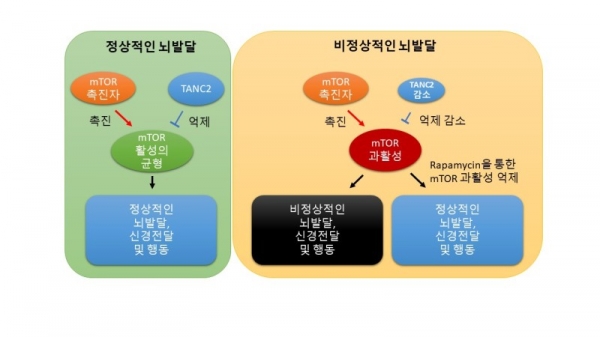
정상적인 뇌발달 상황에서 mTOR의 활성은 촉진자(positive regulator)와 억제자(TANC2; negative regulator)에 의해 균형 있게 조절되며 정상적인 뇌발달, 신경전달 및 행동을 매개한다. 그러나, TANC2의 양이나 기능이 감소하면 그 균형이 깨져서 mTOR의 과활성화가 초래되고 비정상적인 뇌발달, 신경전달 및 행동이 유발된다. 반면 Rapamycin과 같은 mTOR 억제 약물을 투여하면 mTOR 과활성이 억제되고 정상적인 뇌발달, 신경전달 및 행동을 회복시킬 수 있다.
연구진은 TANC2 단백질과 mTOR 신호전달의 관계를 파악하고자 TANC2 발현이 절반으로 줄어든 자폐증 생쥐모델을 제작했다. 실험 결과, TANC2 단백질 결손이 mTOR 신호전달 단백질의 비정상적 과활성화로 이어져 시냅스 및 기억·학습 등의 뇌 기능이 저하되었다. 이때 mTOR 저해 약물인 라파마이신(Rapamycin)을 투여하면 시냅스 및 뇌 인지 기능이 정상으로 회복되었다. TANC2 단백질이 mTOR 신호전달 단백질을 저해하여 뇌 기능을 조절한다는 의미다.
생후 2주령 (Postnatal day 14) 정상 생쥐와 TANC2결손 생쥐의 대뇌 조직에서 mTOR 신호전달 체계에 속한 신호전달 단백질들의 인산화 변화를 비교하였을 때, 특히 mTOR 및 mTOR 하위단계에 있는 단백질들의 활성화 (단백질 인산화의 증가)가 관찰되었으며 (좌측 패널), 이와 상관없는 단백질들은 (우측 패널) 변화가 없는 것을 확인하였다.
TANC2 결손이 신경세포 시냅스의 형성에 영향을 미치는지 확인하기 위해 TANC2 결손 생쥐 뇌의 해마 부위에서 시냅스 기능의 하나인 신경전달 가소성(Long-term potentiation 또는 LTP)을 측정하였을 때 (상단), TANC2 결손 생쥐에서 (HT-Veh) 감소되어 있던 LTP가 Rapamcyin 처리시 (HT-Rapa) 정상으로 회복된다. 정상 생쥐에서는 Rapamycin 처리시 LTP에 변화가 없다 (WT-Veh 및 WT-Rapa). 또한 TANC2 결손 생쥐는 수중미로 실험(하단)에서 기억 및 학습 능력의 감소를 보이는데 (HT-Veh), Rapamycin 처리에 의해 회복됨 (HT-Rapa). 이는 TANC2의 결손이 시냅스 및 뇌인지 기능을 조절하며, Rapamycin이 TANC2 결손으로 초래되는 비정상적 시냅스 및 뇌인지 기능을 회복시킬 수 있음을 의미한다.
나아가 인체의 신경세포에서 TANC2가 줄어들면 mTOR 신호전달체계가 비정상적으로 활성화됨도 발견했다. 인간의 신경계에서도 TANC2가 mTOR 저해인자로서 뇌 발달 및 뇌 기능을 조절하는 것이다.
인체 유래 배아줄기세포인 HuES6 줄기세포로부터 분화시킨 인간 신경세포에서 TANC2 발현을 감소시켰을 때 mTOR 신호전달체계에서 mTOR 하위단계 단백질들인 S6, 4E-BP, GSK3beta의 활성화(인산화)가 증가하는 현상을 보인다. 이는 TANC2의 생쥐뿐만 아니라 인경의 신경세포에서도 mTOR를 억제함을 의미한다.
김은준 단장은 “이번 연구로 최근 자폐 및 뇌 발달장애의 원인으로 부상한 TANC2 유전자 변이의 발병 메커니즘을 밝혔다”며,“후속 연구를 통해 mTOR 신호전달 억제제를 TANC2 유전자 돌연변이에서 기인한 자폐 및 뇌 발달장애의 치료에 활용할 수 있을 것”이라고 전했다.
연구결과는 국제 학술지 네이처 커뮤니케이션즈(Nature Communications, IF 12.121) 온라인판에 지난 5월 11일 18시(한국시간)에 게재되었다.
